Im quantenmechanischen Treibhaus
Birgit Bomfleur, ScienceUp Sturm und Bomfleur GbR,
Camerloherstr. 19, D-85737 Ismaning,
Quanten.de Newsletter, 1. Januar 2003,
ISSN 1618-3770
www.ScienceUp.de
Die Welt wie Muttis Tiefkühltruhe - eine eiskalte Sache. Zum Glück gibts den Treibhauseffekt, der diese maximal für permafrostige Pinguine erfreuliche Situation verhindert.
Die Welt als Sauna - eine hitzige Sache. Zum Glück gibts quantenmechanische Auswahlregeln, die diese maximal für zentralasiatische Wüstenrennmäuse erfreuliche Situation verhindert.
Also: Nur manche mögens heiß - wir Durchschnittsleute lieben es gemäßigt, und deshalb wollen wir zum Jahreswechsel mit einem Glaserl Prosecco (oder ähnlichem) ein Loblied singen auf
die Quantenmechanik und darauf anstoßen.
Ohne quantenmechanische Auswahlregeln würden nämlich Sauerstoff- und Stickstoffmoleküle nicht nur unseren Silvester-Prosecco (oder ähnliches) gehörig erwärmen. Diese Moleküle bilden mit
etwa 99 Prozent den Hauptbestandteil unserer Atmosphäre, aber die Auswahlregeln verhindern, dass sie unser Klima beeinflussen. Dafür
sind Moleküle verantwortlich, die in geringen Mengen in der Atmosphäre vorkommen, also etwa Kohlendioxid (CO2) oder gasförmiges Wasser
(H2O).
Hauptbestandteile der trockenen Atmosphäre
in bodennahen Schichten in Volumenprozent:
Stickstoff N2: 78,08
Sauerstoff O2: 20,95
Argon Ar: 0,93
Kohlendioxid CO2: 0,03
Wir geben gerne zu, dass wir die Situation etwas überspitzt darstellen, aber an Silvester
wollen wir mal nicht zu kleinlich sein. (Darauf noch ein Glaserl Prosecco.) Und das Thema ist auf jeden Fall spannend.
Versuchen wir also herauszufinden, warum manche Stoffe als Treibhausgase wirken, andere hingegen nicht.
Der Treibhauseffekt
Betrachten wir zunächst den Treibhauseffekt. Jeder Körper sendet Energie in Form elektromagnetischer Strahlung verschiedener Wellenlängen aus (Emission), und das tut er umso mehr, je wärmer er ist. Bei hoher Temperatur wird ein erheblicher Anteil im sichtbaren Bereich emittiert. Bestes Beispiel ist die Sonne.
Treffen Sonnenstrahlen auf die Erde, so werden sie zum Teil von Atmosphäre und Erdoberfläche reflektiert. Ein geringer Anteil wird von einigen Molekülen der Atmosphäre "geschluckt" (Absorption, das ist der umgekehrte Vorgang zur Emission), wohingegen ein großer Teil durch die Atmosphäre hindurch geht und erst
von der Erdoberfläche absorbiert wird. Im Fachjargon: Die Atmosphäre ist für die Sonnenstrahlung fast "durchsichtig".
Die Absorption der Sonnenstrahlung führt zu einer Energieerhöhung. Gleichzeitig gibt die Erde auch wieder Energie in Form elektromagnetischer Strahlung ab. Allerdings liegt der Hauptanteil der Strahlung nicht im sichtbaren, sondern im infraroten (IR-)Bereich - schließlich ist die Temperatur der Erde viel niedriger
als die der Sonne. Die IR-Strahlung wird auch als Wärmestrahlung bezeichnet, da sie von der Haut als Wärme empfunden wird.
Damit die Erde sich nicht ständig aufheizt, muss genauso viel Energie wieder in den Weltraum abgegeben werden, wie in das System Erde/Atmosphäre "hineingepumpt" wird.
Es ist bekannt, wie viel Energie der Sonne die Erde erreicht. Daraus können wir mit Hilfe von Modellrechnungen die Temperatur schätzen, die die Erde besitzen muss, um die entsprechende Energie wieder abzugeben: Ohne Atmosphäre wäre die Durchschnittstemperatur lediglich durch die Bilanz zwischen eingestrahlter Sonnenenergie
und der vom Boden abgestrahlten Wärmestrahlung bestimmt: eiskalte -18°C. Zum Glück haben wir eine Atmosphäre, die für eine angenehme Durchschnittstemperatur von etwa 15°C sorgt. Aber Atmosphäre ist nicht gleich Atmosphäre. Bestünde diese nämlich lediglich aus reinem Sauerstoff und Stickstoff, würde sich an den roten Ohren und
klappernden Zähnen nicht viel ändern. Erst eine kleine Prise sogenannter Treibhausgase in unserer Lufthülle sorgt bei uns für erträgliche Temperaturen. Wichtigste Vertreter dieser Gase sind Wasserdampf und Kohlendioxid. Diese Moleküle absorbieren Strahlung im IR-Bereich, sie werden dadurch in Schwingung versetzt - und die Atmosphäre erwärmt sich.
Entsprechend ihrer Temperatur strahlt die Atmosphäre wieder Wärme ab. Natürlich in alle Richtungen gleichmäßig. Und eben auch wieder in Richtung Erde. Hätte die Erde nun die oben erwähnte, berechnete Temperatur von -18°C, so würde aufgrund des Rückkopplungsprozesses die von dem System Erde/Atmosphäre in den Weltraum abgegebene
Energie geringer sein als die von der Sonne aufgenommene. Also erwärmt sich die Erde so lange, bis die gesamte Energiemenge, die in den Weltraum verschwindet, der aufgenommenen Energie entspricht. Und schon haben wir 15°C.
Ähnliches passiert in den holländischen Treibhäusern. Die Glasdächer sind durchsichtig für die Sonnenstrahlung. Die Glasbedeckung absorbiert aber die aus dem Treibhaus emittierte IR-Strahlung und strahlt Wärme wieder zurück ins Treibhaus - die "Tomaten" gedeihen. Übrigens: Die Bezeichnung Treibhauseffekt" wurde direkt aus den Gemüsehäusern
in die Atmosphäre exportiert (darauf kein Glaserl Prosecco, sondern eine Bloody Mary) - auch wenn die Vorgänge zwischen Sonne und Erde viel komplizierter sind als im Gemüse-Zuchthaus.
Der Treibhauseffekt ist also lebensnotwendig - es sei denn, man verstärkt ihn. Der Mensch feuert durch seine kurzsichtige Energiepolitik Treibhausgase in die Atmosphäre. Besonders relevant ist das Kohlendioxid, dass durch Verbrennung fossiler Brennstoffe wie Erdöl oder Kohle entsteht. Die meisten Wissenschaftler sind sich einig, dass durch die rasante
Erhöhung der Konzentration der Treibhausgase sich die Erde erwärmt, was zu dramatischen Klimaproblemen führen wird.
Quantenmechanisches Treibhaus
Warum nehmen Sauerstoff- oder Stickstoffmoleküle nicht an diesem Spiel teil? Durch Absorption von Strahlung im infraroten Bereich werden Molekülschwingungen angeregt. Nach der Quantenmechanik sind für die Schwingungen nur genau definierte Energiewerte
zulässig, die Schwingung ist gequantelt. Wie wir sehen werden, haben auch Sauerstoff und Stickstoff Schwingungsniveaus im infraroten Bereich. Ob aber ein Übergang zwischen den Schwingungsniveaus durch Absorption elektromagnetischer Strahlung angeregt
werden darf - man spricht dann von erlaubten Übergängen -, wird durch die quantenmechanischen Auswahlregeln festgelegt. Moleküle, deren Schwingungsübergänge verboten sind, bezeichnet man auch als IR-inaktiv.
In Abbildung 1 ist die Potenzialkurve eines zweiatomigen Moleküls skizziert, das um den Gleichgewichtsabstand r0 schwingt. Im Grundzustand befindet sich das Molekül in dem Zustand mit der Quantenzahl n = 0. Durch Absorption eines Lichtquants kann
es in den ersten angeregten Zustand mit der Quantenzahl n = 1 angeregt werden. Die Energie E des Lichtquants muss dabei der Energiedifferenz zwischen diesen beiden Zuständen entsprechen. Durch die Beziehung E = h f ist damit die Frequenz f des Lichtquants,
also des Photons festgelegt. h ist die Plancksche Konstante. Durch Emission eines gleich großen Lichtquants kann das System wieder in den Grundzustand zurückkehren. Die Energiedifferenzen zwischen den unteren Schwingungsniveaus sind charakteristisch für ein
Molekül und liegen im Allgemeinen im IR-Bereich.
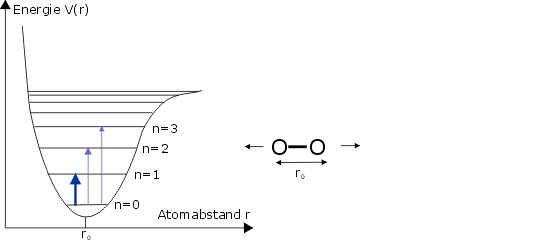
Abbildung 1: Potenzialkurve mit Schwingungsniveaus (links) und Schwingung (rechts) des zweiatomigen Sauerstoffmoleküls O2.
Der dicke blaue Pfeil symbolisiert einen Absorptionsvorgang vom Grundzustand in den ersten angeregten Zustand.
Die beiden anderen Vorgänge sind "fast" verboten, die Übergangswahrscheinlichkeit ist sehr gering.
Ein mehratomiges Molekül kann auf verschiedene Arten schwingen. In Abbildung 2 sind die verschiedenen Schwingungsmöglichkeiten
von Wasser skizziert. Jede dieser Schwingung kann durch eine eigene Potentialkurve wie in Abbildung 2 beschrieben werden. Die
Energiedifferenzen zwischen den Niveaus ist für jede Schwingung eine andere.

Abbildung 2: Die Schwingungen eines Wassermoleküls
Natürlich kann man auch für Stickstoff und Sauerstoff eine analoge Potenzialkurve und die zugehörigen Schwingungsniveaus wie in
Abbildung 2 ermitteln. Die Energiedifferenzen zwischen dem Grundzustand und dem ersten angeregten Zustand liegen ebenfalls im
infraroten Bereich.
Die Absorption und Emission elektromagnetischer Strahlung wird mittels der sogenannten Störungstheorie behandelt. Man erhält dadurch
die Wahrscheinlichkeiten für einen Übergang und somit die Auswahlregeln.
Die speziellen Auswahlregeln geben die Änderungen der Quantenzahlen an, die bei einem Übergang erlaubt sind. Für Schwingungen sind
Übergänge mit n = ±1 erlaubt. Oberschwingungen mit n = ±2,±3,... sind zwar nicht verboten, treten aber mit geringer Wahrscheinlichkeit auf.
Diese Auswahlregeln machen jedoch noch keine Aussagen darüber, ob ein Molekül IR-aktiv oder -inaktiv ist.
Eine weitere Untersuchung der Übergänge mittels der Störungstheorie führt uns zu den allgemeinen Auswahlregeln. Diese geben eine bestimmte Eigenschaft an,
die ein Molekül haben muss, damit der betrachtete Übergang überhaupt möglich ist. Für Schwingungsübergänge lautet die allgemeine Auswahlregel: Das Dipolmoment -
die Beschreibung der Ladungsverteilung - muss sich bei einer Auslenkung entlang der Schwingungskoordinate ändern.
So, da haben wir es. Sauerstoff ist ein zweiatomiges Molekül aus gleichen Atomen (homonuklear) ohne Dipolmoment. Wenn das Molekül schwingt, sich also die Bindung streckt und staut,
entsteht auch kein Dipolmoment. Somit ändert sich auch das Dipolmoment nicht während der Schwingung. Sauerstoff ist IR-inaktiv. Diese Betrachtung gilt ganz allgemein für zweiatomige homonukleare Moleküle, also auch für Stickstoff.
Anders sieht's zum Beispiel beim Wasser aus. Bei jeder der drei möglichen Schwingungen ändert sich das Dipolmoment, alle drei Schwingungen sind IR-aktiv. Beim linear gebauten Kohlendioxid ist die symmetrische Streckschwingung entlang
der Molekülachse IR-inaktiv, die restlichen Schwingungen sind jedoch IR-aktiv. Wasser und Kohlendioxid tragen somit zum Treibhauseffekt bei, Sauerstoff und Stickstoff nicht.
Und jetzt wird gefeiert. Lassen wir viele Raketen knallen, um den Treibhauseffekt weiter anzuregen. Immerhin hat das ja auch sein Gutes: Wir können im nächsten Sommer den Badeanzug - ein Weihnachtsgeschenk von Tante Hildchen - so richtig benutzen. Darauf - hicks! - noch ein letztes Glaserl (??) Prosecco.
Birgit Bomfleur
Sie können auch eine PDF-Version dieses Artikels abrufen.
© 2002 ScienceUp Sturm und Bomfleur GbR, Alle Rechte vorbehalten. Nichtkommerzieller Nachdruck und Wiedergabe gestattet bei Quellenangabe
ScienceUp Sturm und Bomfleur GbR, www.ScienceUp.de
Ein Buchtipp hierzu:


"Schon wieder Bilder von Überschwemmungen in den Medien. Menschen, die Sandsäcke schleppen.
Überflutete Keller, zerstörte Existenzen. Alles doch gerade erst gesehen, oder? Man stumpft ab...
NEIN! Das darf nicht sein, die Flut betrifft uns alle. Die Katastrophen sind hausgemacht, der Klimawechsel hat bereits begonnen.
Jörg Kachelmann, der bekannteste unter den TV-Wetterfröschen, stellt mit diesem
Taschenbuch eine umfangreiche Sammlung von Fachaufsätzen zur Verfügung. Wer also ein
"Kachelmann"-Buch erwartet, wird enttäuscht sein, da der Herausgeber Jörg Kachelmann
selbst nur ein kurzes Vorwort geschrieben hat. Die anderen Autoren sind Ökologen, Journalisten und Politiker,
die das Thema Klimawandel unter verschiedenen Aspekten ausführlich behandeln. Sehr lesenswert für
jeden, dem die oft oberflächliche Diskussion in den Medien nicht (mehr) genügt."
(G.Sturm)
Taschenbuch, rowohlt (2002), ISBN 3498035177
Mehr Infos bei Amazon.de


